2024.05.13
金属のイオン化傾向についてイオンからやさしく解説!語呂合わせでの覚え方も紹介

本記事のテーマはイオン化傾向についてです。高校化学で「金属のイオン化傾向」を学習しますが、中学生の理科でも化学電池の電極の組み合わせとして「イオンになりやすい金属・なりにくい金属」を学習します。
イオンは目に見えるものではないため、「イオン化って何?」「イオン化傾向がわからない」という方も多いのではないでしょうか。
そこで本記事では、金属の反応性や性質について解説し、なぜイオン化傾向が重要なのかと語呂合わせでの覚え方についても紹介します。
イオンとは?
まずは、イオンとは何なのか?について簡単に紹介します。
イオンとは、原子が電気を帯びた状態のことを指します。
通常、原子には、プラスの電気を帯びている陽子と、マイナスの電気を帯びている電子が同じ数だけ存在し、バランスが取れた中性な状態を保っています。
しかし、何らかのきっかけで電子が出入りすると、電子が足りない状態(=陽イオン)や、電子が多い状態(=陰イオン)となり、正または負の電気を帯びるようになります。これらの状態を合わせてイオンと言います。
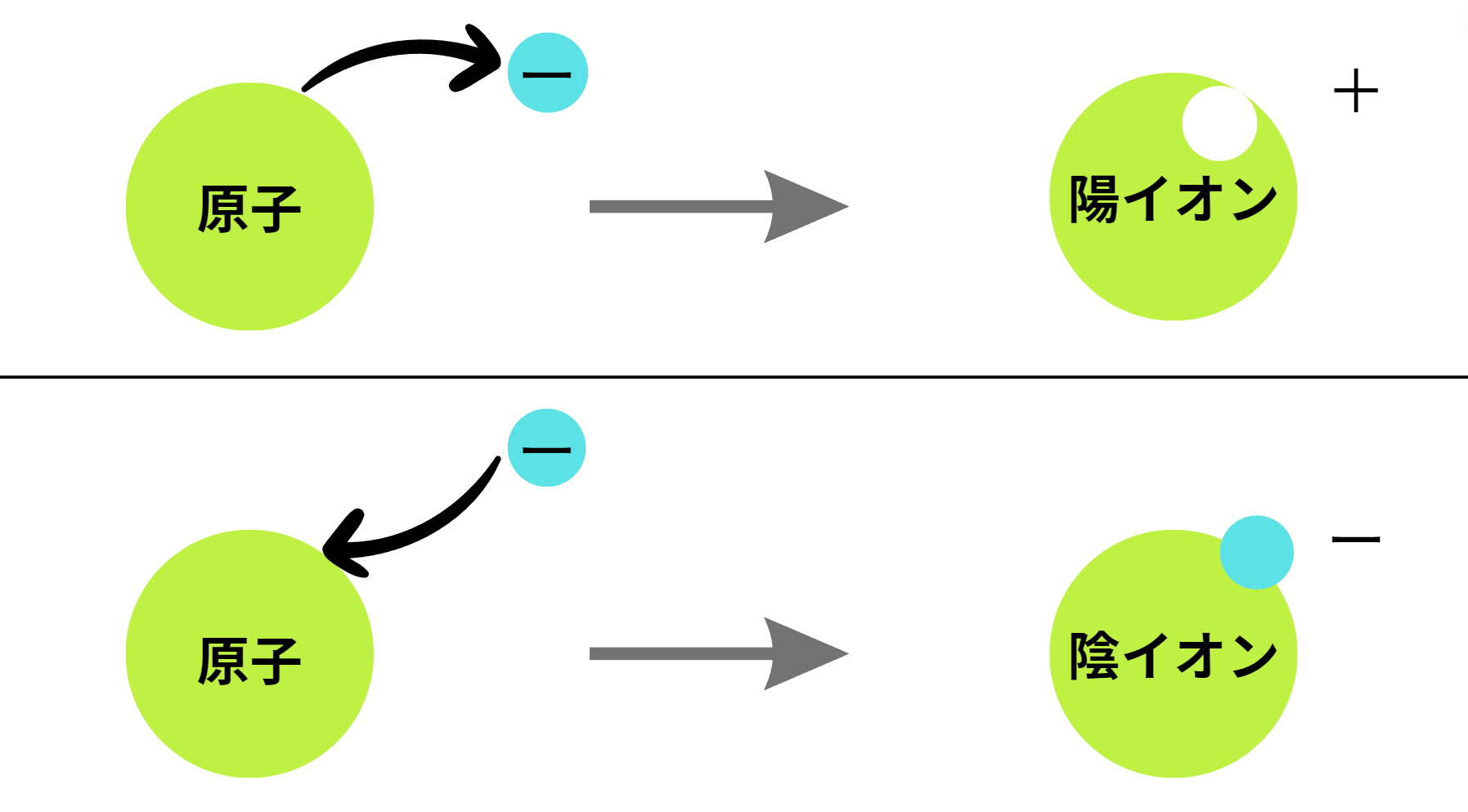
イオンになり電気的にプラスやマイナスになると、水に溶けやすくなったり電池としての性質を持ったりするようになります。
イオン化傾向とは?
イオン化傾向とはその文字の通り、「イオン化しやすい傾向」を意味します。具体的には、金属(金属単体の原子)が空気中や水、水溶液の中で陽イオンになりやすいかどうかを意味します。
陽イオンになるということは、電子を放出するということなので、イオン化傾向の高さ=電子の放出しやすさと理解しましょう。
また、電子を放出することを「酸化される」と言うため、イオン化傾向が高い金属は酸化されやすいと言えます。さらに、酸化されやすい=相手を還元しやすいと言えるため、イオン化傾向が高い金属は、強い還元力を持つとも言えます。
イオン化傾向の覚え方
イオン化傾向、つまり陽イオンへのなりやすさは金属原子毎に異なります。
イオン化傾向の大小の決定には、金属原子の電子の配列やイオン半径の大きさなどさまざまな要因が影響し、これを正確に理解するためには大学以上の範囲を学習する必要があります。
しかし、中学や高校の理科でも、イオン化傾向に基づく問題が出題されるため、これを覚える必要があります。今回は、イオン化傾向を高い順に覚えるための有名な語呂合わせを紹介します。
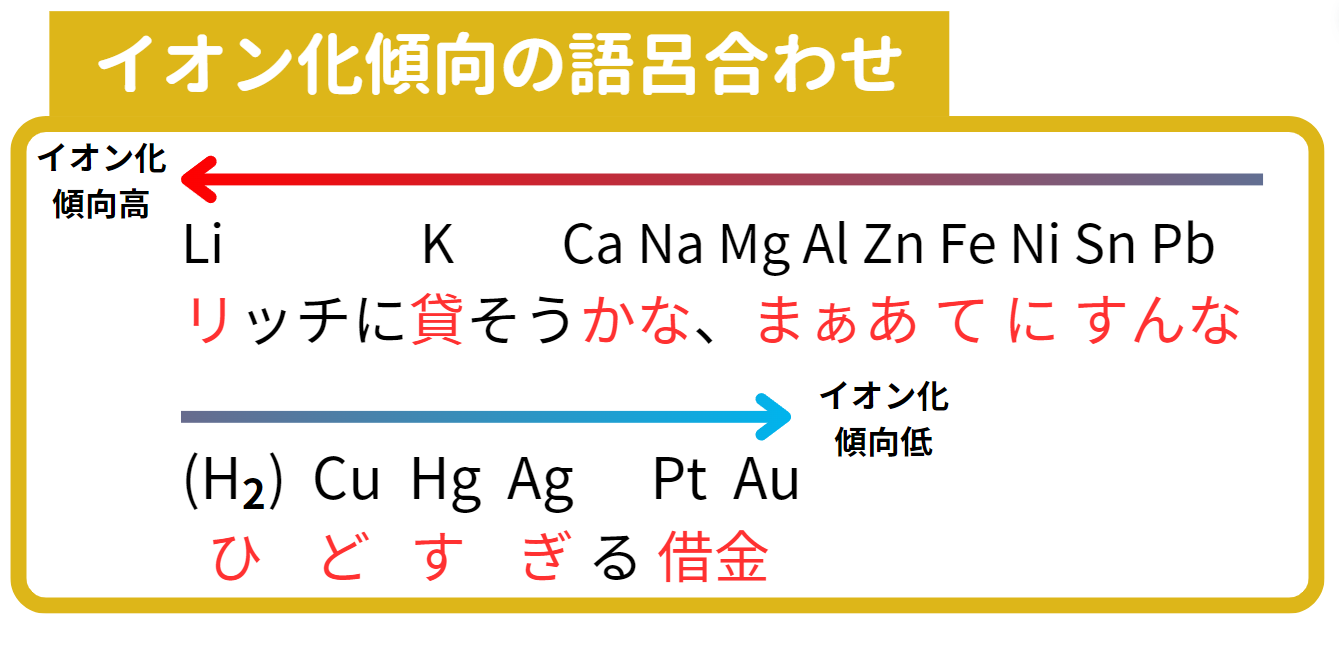
イオン化傾向の覚え方は以下の通りです。
リッチ(リチウム)に貸(カリウム)そうか(カルシウム)な(ナトリウム)、
ま(マグネシウム)ぁ(アルミニウム)あ(亜鉛)て(鉄)に(ニッケル)すん(スズ)な(鉛)
ひ(H2=水素)ど(銅)すぎ(水銀)る借金(白金・金)
この中では、リチウムが一番イオン化傾向が高く(陽イオンになりやすい)、次にカリウム、カルシウムと続き、金が一番イオン化傾向が低い(陽イオンになりにくい)と言うことになります。
白金の部分を「しゃっきん」としていたりと、こじつけも多いですが、暗記が必須のイオン化傾向なので、しっかりと覚えるようにしましょう。
なお、H2(水素)が括弧で囲まれているのは、金属ではないからです。しかし、水溶液中での電子のやり取りを考えるうえで重要になるため、ここに含まれています。
イオン化傾向による金属と水の反応性
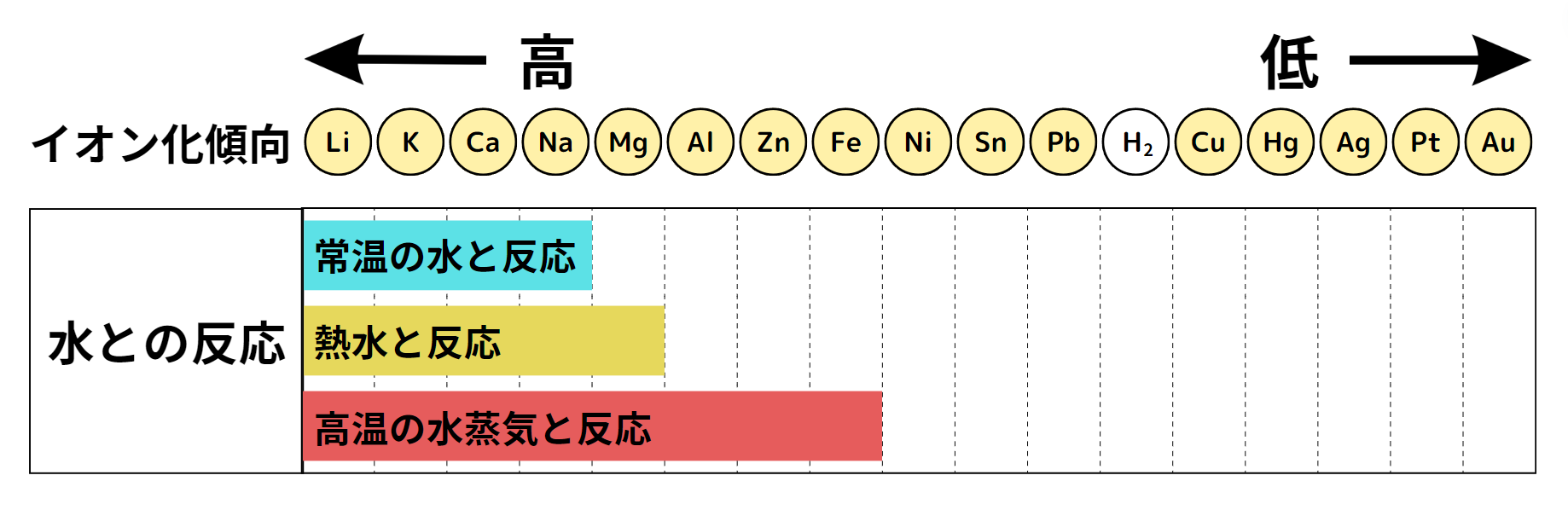
イオン化傾向と、金属と水の化学反応のしやすさには関係があり、イオン化傾向が高ければ高いほど、水と反応しやすいです。
イオン化傾向の差によって、エネルギーがさほどない常温の水とも化学反応する金属や、エネルギーが高い熱水や高温な水蒸気でしか化学反応しない金属があるため、覚えておきましょう。
常温の水で反応
ナトリウム以上のイオン化傾向を持つLi, K, Ca, Naは常温で反応し、水素を発生して水酸化物となります。水溶液には水酸化物イオンが残るため塩基性を示します。
Ca + 2H2O → Ca(OH)2 + H2
2Na + 2H2O → 2NaOH + H2
熱水で反応
イオン化傾向の順でNaの次である、Mgは常温の水では反応しませんが、熱水(沸騰した水)と反応します。
Mg + 2H2O → Mg(OH)2 + H2
高温の水蒸気と反応
Mgより低いイオン化傾向の金属であるAl, Zn, Feは、高温の水蒸気と反応します。
2Al + 3H2O → Al2O3 + 3H2
イオン化傾向による金属と酸の反応性
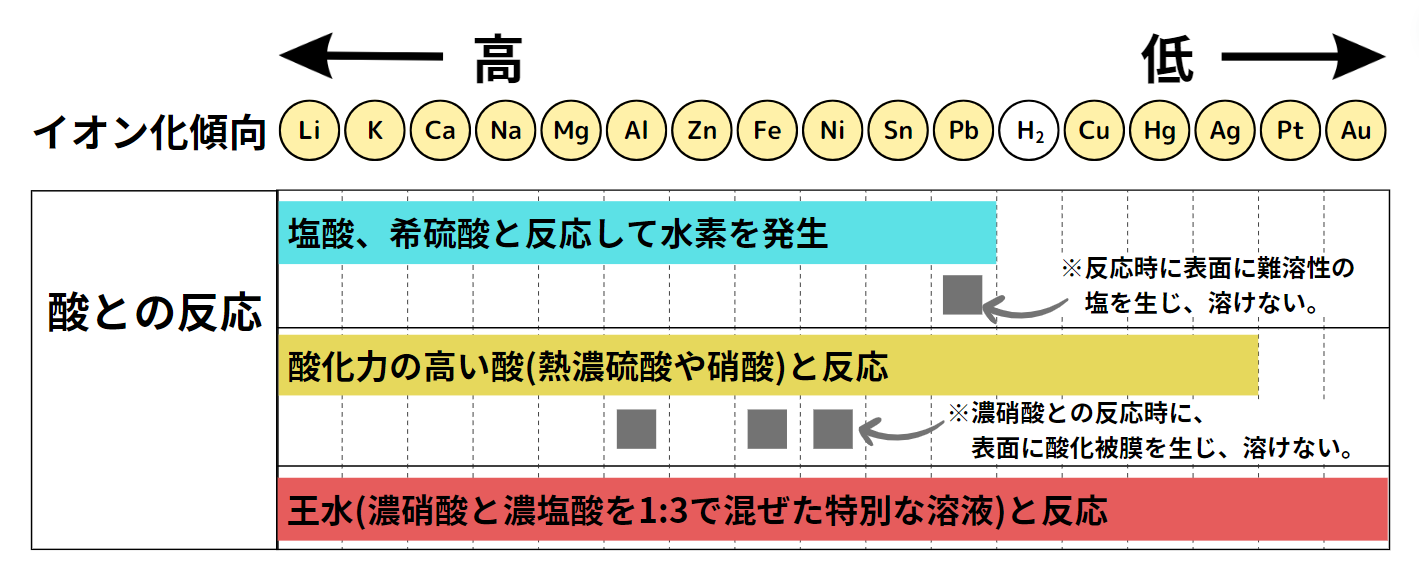
水素よりもイオン化傾向の高い金属は水素より強い還元力を持つため、水素イオンH+を水素H2に還元できます。そのためこれらの金属は塩酸などの酸と反応し、水素を発生しながら溶けます。
Zn + 2HCl → ZnCl2 + H2
ただし鉛(Pb)は例外として、希塩酸と希硫酸と反応はしますが、反応により表面に生成される塩が難溶性であるため、反応が止まり、溶けません。
〇×問題で「鉛は塩酸と反応し溶ける」といった問題がある場合、「溶けない」が正解になるため注意しましょう。
酸化力の高い酸との反応
H2よりイオン化傾向の低い金属であっても、熱濃硫酸や硝酸などの強い酸化力を持つ溶液とは反応します。ただし、PtとAuは「王水」という濃硝酸と濃塩酸を1:3で混ぜた特別な溶液にしか溶けないことを覚えておきましょう。
また、アルミニウム(Al), 鉄(Fe), ニッケル(Ni) については、濃硝酸と反応はしますが、表面に緻密な酸化被膜が形成され、反応が進まなくなります。この状態を不動態と言います。
鉛における反応と同様、「アルミニウムは濃硝酸に溶ける」は不正解なため注意しましょう。
イオン化傾向を応用したメッキ
金属は空気中や水中の酸素などによって酸化されると、さびてしまいます。
その「さび」を防ぐために、金属の表面を別の金属で薄く覆ってしまうという方法があり、これをメッキと言います。
メッキの代表例であるトタンとブリキを紹介します。
さびにくいトタン
トタンは「トタン屋根」という言葉があるように、屋根などに使われるメッキです。トタンは、鉄(Fe)を亜鉛(Zn)で覆って作られます。
ZnはFeよりイオン化傾向が大きいため、Fe単体のときより表面がさびやすいです。ではなぜわざわざZnでメッキをするのでしょうか。
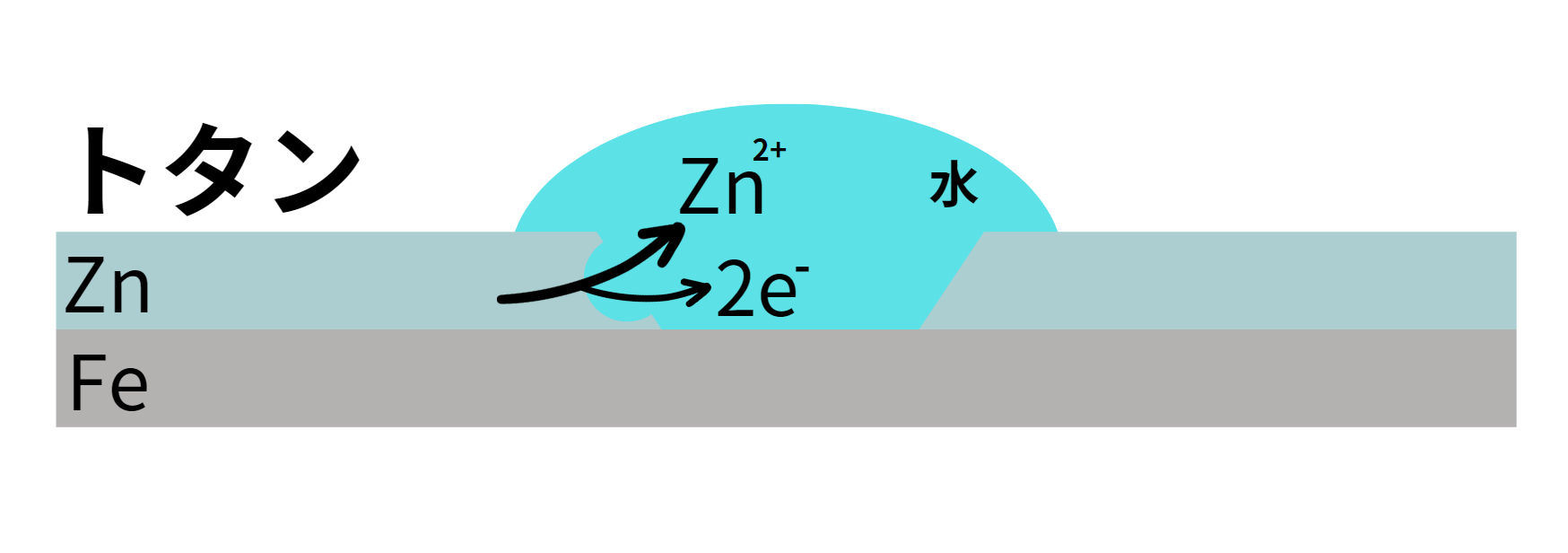
トタンに傷がついてFeが露出したときに、イオン化傾向がより高いZnが、Feがさびる前に酸化し、表面に酸化被膜を生成してくれます。
そのため、トタンは雨風にさらされ傷つきやすい屋根などに使われることが多いです。
傷がつきにくいブリキ
ブリキは「ブリキのおもちゃ」という言葉があるようにおもちゃや缶詰などに使われるメッキです。ブリキは鉄(Fe)をスズ(Sn)で覆って作られます。
SnはFeよりもイオン化傾向が小さいため、Fe単体よりも表面がさびにくくなります。
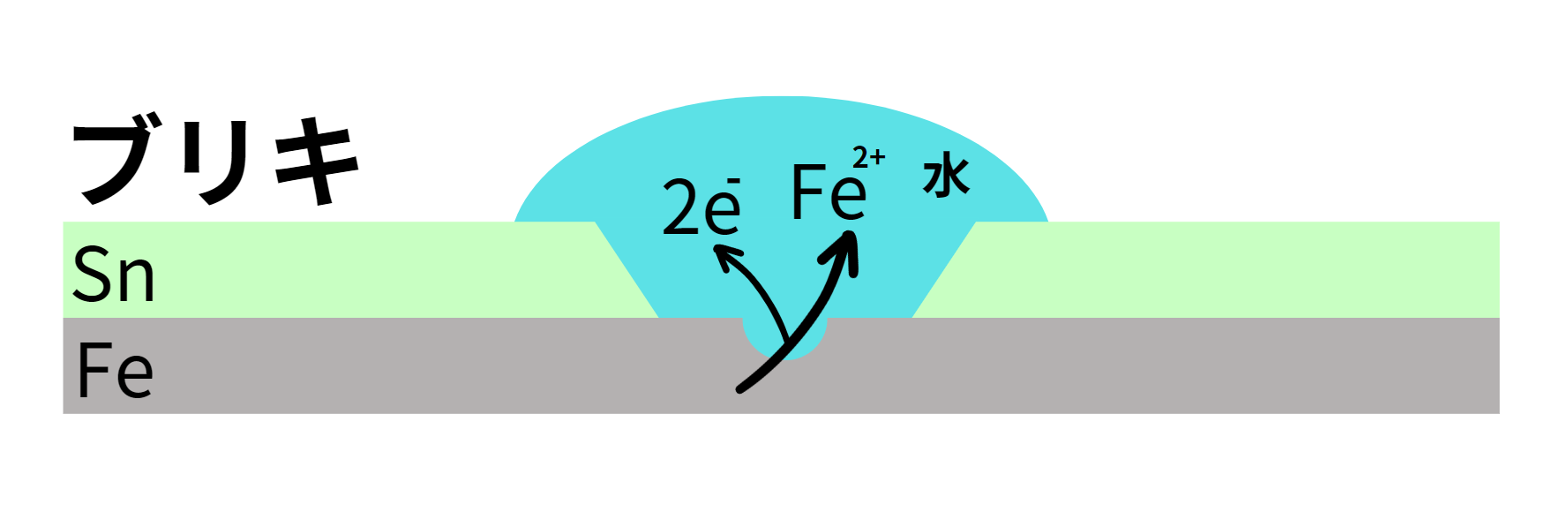
しかし一方で、傷がついた場合にはSnよりもFeのほうが先にさびていってしまうという欠点はあります。
鉄よりも表面がさびにくいブリキは、子供のおもちゃや、内側に傷がつきにくい缶詰などに利用されています。
まとめ
いかがでしたでしょうか。本記事では、イオン化傾向の説明と覚え方の語呂合わせについて解説しました。
イオン化傾向はその順番を覚えるだけでなく、水や酸との反応や、メッキなどでも重要になる性質です。
まずはイオンとは何か、イオン化傾向とは何かを理解し、今回紹介した語呂合わせを活用して、自分のものにしましょう。
教室数・生徒数No.1の個別指導塾!
明光義塾では、勉強の進め方や、勉強計画の立て方など、学習の質を高めるための豊富なノウハウを持っています。お子さまの抱える課題に向き合いながら、目標に向かって効率的な勉強を行えるようサポートできます。
お子さまの現状の課題を知りたい方、お子さまの更なる成長をお考えの方は、ぜひ一度お近くの明光義塾までお気軽にご相談ください。
この記事を家族や友人に教える
明光プラスで読みたい記事のテーマを募集
明光プラスでは読者の方のご期待に沿えるように読みたい記事のテーマを募集しています。ぜひ下のリンクからアンケートにお答えください。
あわせて読みたい記事
-

炎色反応の仕組みと利用方法をやさしく解説!語呂合わせでの覚え方も紹介
2024.11.27
本記事のテーマは炎色反応についてです。主に中学の化学の応用や高校の化学基礎で学習します。 炎色反応と一口に言っても、それぞれの金属にそれぞれ違う色の炎の反応が出るため覚えにくく苦手意識を持つ方や、反...
-

等比数列は簡単!一般項や和の公式を1から解説します
2025.06.06
数Bの数列を学習すると等差数列の次に学ぶのが等比数列です。しかし等比数列に比べて見た目が複雑で規則性も掴みにくいため、苦手意識を持っている人も多いのではないでしょうか。等比数列は漸化式の問題を解くと...
-

部分分数分解は簡単!やり方と公式を3つのパターンと4つのステップでやさしく解説します!
2025.05.01
部分分数分解という言葉自体がややこしく苦手意識を持っている方も多いのではないでしょうか。 数Ⅲの積分で部分分数分解が必要になることもあり、大学入試で出ることもあるためしっかりと理解しておきたいところ...
タグ一覧
おすすめ記事
-

自主学習のネタの決め方・ノートの書き方を解説!
2025.05.29
学校から自主学習をするようにと言われて、「何をすればいいの?」「進め方があってるのか不安」と悩まれているご家庭も多いことでしょう。 そこでこの記事では、そもそも自主学習をする目的、ネタの探し方・決め...
-

歴史の勉強法のコツを紹介!楽しく覚える方法も解説します!
2024.04.30
歴史の勉強について、どんな印象を持っていますか? 「覚えることが多い」「つまらない」「勉強する意味がわからない」。 歴史の勉強に苦手意識を持っている人は、このように捉えていることが多いです。...
-

テスト勉強してない!不安な中でも前日・当日にできることとは?
2022.06.15
翌日に迫ったテスト。「勉強してない!」と焦り出したとき、一体どのように対策すればよいのでしょうか。 勉強は日ごろの積み重ねによって力がついてくるものです。テスト勉強もスケジュールを立てて計画...
-

小学生に塾は必要か?中学受験しない場合の塾の必要性は?
2021.12.08
お子さまがいると、「小学生のうちから塾に通わせたほうがいいの?」と教育の方針に悩むことが多いでしょう。小学生からの塾は、中学受験をしないのであれば不要だといわれることもありますが、通わせるこ...
-

模試の勉強法とは?模試の成績の上げ方から年代別の受験への活かし方まで
2021.10.12
模試は、志望校合格のために必ずといってよいほど受けるべきものです。 しかし、模試をどのように活用すればよいのか分からない、という人も多いでしょう。 この記事では模試を受けるメリットや成績を上...
-

定期テスト(中間テスト・期末テスト)の勉強はいつから始める?高得点を狙える勉強法とは
2021.02.22
定期テストの勉強はいつから始めていますか?定期テストの結果は、1年の成績を大きく左右するうえ、内申にも直結します。そのため受験を視野に入れた勉強では、学力を高めることと同時に、定期テストで高...









